国家卫健委通知数据造假将承担法律责任
近日,国家卫健委发布《关于加强卫生健康统计工作的指导意见》(以下简称《意见》)。
近日,国家卫健委发布《关于加强卫生健康统计工作的指导意见》(以下简称《意见》)。
近日,广州市市场监督管理局发布《广东省医疗器械注册人制度试点务实创新 助推广东医疗器械产业高质量发展》一文显示,广东省医疗器械注册人制度试点自2018年8月14日开始落地实施,试点工作实施两年以来,全省共有62个试点品种获准上市,已受理70多家企业近300个品种开展审评,另有100家企业近500个品种有意向参与试点。
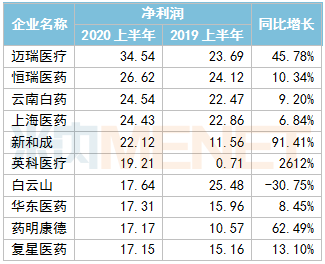
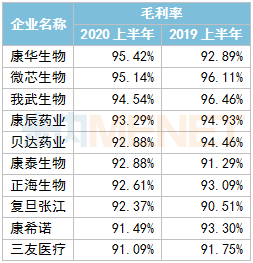
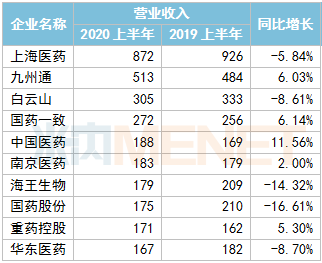
截至目前,339家A股医药企业已披露了2020年上半年业绩情况,上海医药、九州通等16家营收超百亿元;迈瑞医疗、恒瑞医药、云南白药等20家净利润超10亿元;康华生物、微芯生物、我武生物、康辰药业等14家毛利率超90%。值得一提的是,受新冠肺炎疫情影响,一季度有超过50%的企业业绩(营收、净利润)双跌,53家净利润亏损;二季度随着国内疫情防控常态化,生产逐步复苏,经济正有序恢复,一些领域的刚性需求迎来了反弹。上半年业绩双跌的企业下滑至42%;43家药企净利润亏损,而同比去年同期净利润亏损仅有17家。
近日,四川省医保局发布《四川省药品和医用耗材集中采购货款在线支付结算管理办法(暂行)(征求意见稿)》显示,四川省医保局开设药械货款集中支付监管账户,专项用于办理并监管医药机构与医药企业通过平台开展的药械采购货款收付业务。
8月31日,贵州省公共资源交易中心发布贵州、重庆、海南三省(市)联盟《关于公示冠脉球囊集中采购企业审核结果及企业代表品的通知》(下称《通知》),公示参加本次带量采购的企业名单,以及对应产品最低价。
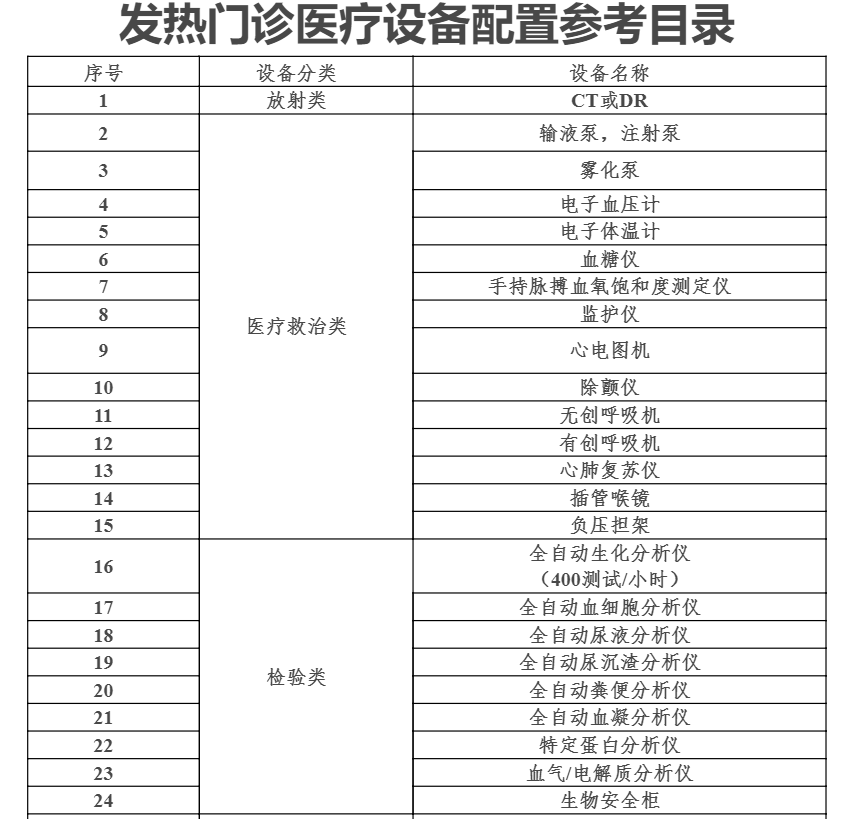
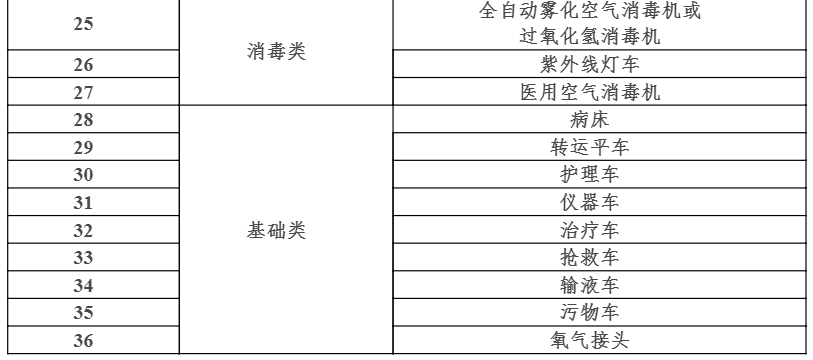
8月31日,国家卫健委规划发展与信息化司发布《发热门诊建筑装备技术导则(试行)》(下称《技术导则》),适用于医院发热门诊的新建、改建和扩建项目。
8月31日,辽宁省药监局消息,省药监局组织开展对进口医疗器械代理人监督检查,按照医疗器械年度监督检查计划,省药监局已于近期启动对对我省进口医疗器械代理人的监督检查。

8月31日,国家卫健委和国家发展改革委联合印发了《发热门诊建筑装备技术导则(试行)》,这也是目前最新的发热门诊建筑装备指导规范,适用于医院发热门诊的新建、改建和扩建项目。
2020 年上半年,新冠疫情在全球范围的爆发,使得部分医疗器械各个国家成为急需补给的产品,大到CT、呼吸机,小到口罩、到测温仪。经过此轮疫情的考验,国内和国际市场的格局开始重新洗牌。
带量采购是一盘大棋