浅析国内直线加速器、伽玛刀细分领域发展状况
国家局2021年度第一批药械组合产品属性界定结果汇总

2021年度第一批药械组合产品属性界定结果汇总
本次汇总2020年12月1日至2021年5月31日期间的药械组合产品属性界定结果。相关产品属性界定结果是基于申请人提供的资料得出,不代表对其产品安全性和有效性的认可,仅作为该产品申报注册的参考。




医疗器械标准管理研究所
2021年7月7日
文章来源于疗器械标准管理研究所,全文由整理。医疗是一家全球医疗器械3C产业平台,提供医疗器械注册、医疗器械临床、医疗器械CRO、医疗器械CE认证、医疗器械委托生产等一站式服务,欢迎咨询。…
山东省医疗器械行政处罚裁量基准 附官司方解读
《山东省医疗器械行政处罚裁量基准》(以下称《裁量基准》)解读如下:
一、修订的必要性
规范行政处罚自由裁量权,建立健全行政裁量权基准制度是党的十八届四中全会关于坚持严格规范公正文明执法的重要内容,也是推进依法治国,建设法治政府的一项重要工作任务。自2015年原食品药品监督管理局制定发布医疗器械行政处罚裁量基准以来,对规范我省医疗器械行政处罚裁量权起到了积极的作用。
2020年12月21日,国务院第119次常务会议修订通过了《医疗器械监督管理条例》,并于2021年6月1日起施行。修订后的条例严格落实“四个最严”要求,加大了对违法行为的处罚力度,大幅度提高罚款数额,增加了处罚到人的规定,与之前的《医疗器械监督管理条例》相比有了很大变化。为指导全省医疗器械监管部门准确适用《医疗器械监督管理条例》,进一步规范行政处罚裁量行为,需要对原有的医疗器械行政处罚裁量基准进行调整完善,以保证行政处罚行为合法、适当。
二、起草过程
我局3月组织起草工作,4月20日形成初稿,书面征求了各市市场监管局、省局相关处室、各检查分局和相关直属单位的意见,并在省局网站公开征求社会公众意见。期间共收到意见建议11条,经认真研究采纳吸收了2条。在进一步修改并经法制机构合法性和公平竞争审查后,由局务会审议通过。
三、需要说明的几个问题
《裁量基准》包含处罚裁量基准15个,每一个都细化为违法情形、处罚依据、处罚种类、实施主体、裁量范围和处罚标准。
(一)关于处罚标准的把握
《裁量基准》把“裁量阶次”划分为4个,即中限、减轻、从轻和从重。其中,从轻、中限、从重三个“裁量阶次”分别对应低限、中限、高限,是对法定处罚区间按照3:4:3的比例进行划分的。由于《医疗器械监督管理条例》中,既有一般违法情形,又有严重违法情形,还有很多罚则明确情节严重的,要“处罚到个人”,条文规定比较复杂,仅靠4个阶次不能完全划分清楚。为解决这一问题,我们先通过“裁量基准”区分“对单位”(含一般情节和严重情节)和“对个人”,再将其体现到4个“裁量阶次”中,因此有些条款会出现每个阶次中,既有对企业的处罚标准,又有对个人的处罚标准。
(二)关于裁量范围中处罚种类的把握
“裁量范围”仅针对“罚款”的处罚种类,对于警告、没收违法所得和非法财物、吊销批准证明文件、许可证等行政处罚种类未予纳入,主要基于以下考虑:一是在山东省药品和化妆品行政处罚裁量基准制定过程中,经广泛讨论已形成共识,认为处罚种类在法律规范中规定非常明确,且不具有自由裁量性,故不可随意进行减少。本次对医疗器械的法定处罚种类不予裁量,既有利于实现药械化监管政策的连续性,同时也与药品和化妆品裁量基准的体例保持一致;二是如对处罚种类予以裁量,将会出现执法人员将没收、罚款等某一个或某几个罚种减掉的可能性,具有较大的执法风险,同时也不符合“四个最严”要求。
(三)减轻处罚幅度的把握
《行政处罚法》规定了特定情况下,应当减轻处罚。为保持药械化监管的连续性、一致性,我们沿用了之前药品和化妆品行政处罚裁量基准中关于减轻的原则规定,即把减轻处罚的裁量幅度允许减到最低限度的10%,作为减轻的底线,避免实践中发生减轻到“零”的可能性。
(四)关于施行日期的说明
本基准自2021年6月15日起施行,有效期至2026年6月14日。因修订后的《医疗器械监督管理条例》将于2021年6月1日起正式施行,为了指导全省医疗器械监管部门准确适用法规,规范行政处罚裁量行为,基准施行日期与印发日期的间隔我们做了适当调整,目的在于保障行政处罚行为合法、适当。
通知原文如下:

山东省药品监督管理局关于印发山东省医疗器械行政处罚裁量基准的通知
2021-06-08
鲁药监规〔2021〕6号
山东省药品监督管理局关于印发山东省医疗器械行政处罚裁量基准的通知
各市市场监督管理局,省局机关各处室、各检查分局、执法监察局:
现将《山东省医疗器械行政处罚裁量基准》印发给你们,请遵照执行。执行中如有问题,请及时向省局反馈。本基准自2021年6月15日起施行,有效期至2026年6月14日。
山东省药品监督管理局
2021年5月31日
(公开属性:主动公开)
山东省医疗器械行政处罚裁量基准
说 明
1.本裁量基准中,处罚幅度裁量采用的方法是按照行政处罚裁量的通行做法,将裁量区间划分为0-30%、30%-70%、70%-100%三段,分别对应处罚幅度的低限、中限、高限。计算方式是,假设罚款的裁量区间最低值为A,最高值为B,那么中限阶次取值范围的最低值为A+(B-A)×0.3,最高值为B-(B-A)×0.3;减轻阶次取值范围的最低值为0.1A,最高值为A;从轻阶次裁量因素第一栏取值范围的最低值为A,最高值为A+(B-A)×0.3;从轻阶次裁量因素第二栏为A;从重阶次裁量因素第一栏取值范围的最低值为B-(B-A)×0.3,最高值为B;从重阶次裁量因素第二栏为B。…
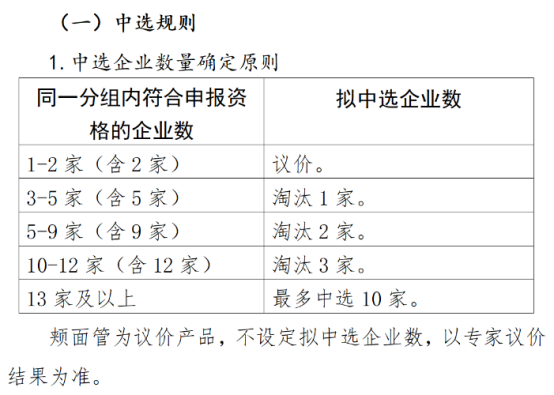
非医保覆盖集采,直指口腔正畸!牙科“暴利”故事将终结!

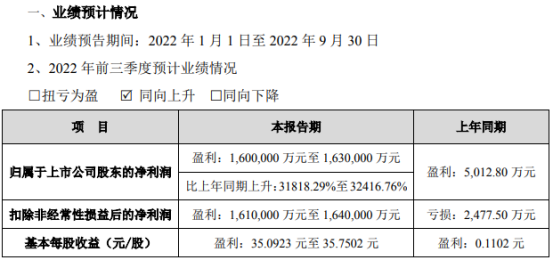
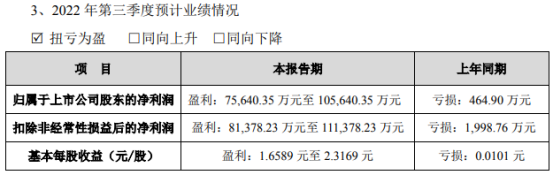
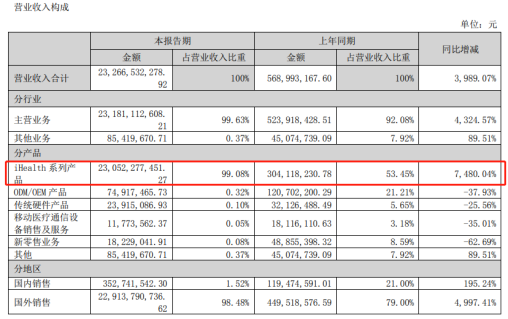
IVD上市公司业绩分化!九安医疗净利暴涨300倍成三季报“预增王”
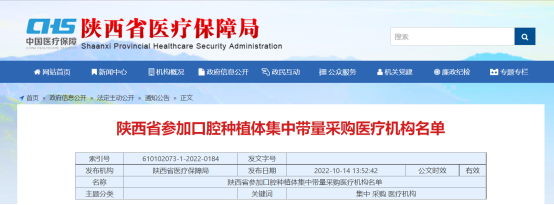
种植牙之后,15省口腔正畸托槽集采来了!
国家药监局批准注册222个医疗器械产品公告
序号 | 产品名称 | 注册人名称 | 注册证编号 |
境内第三类医疗器械 | |||
1 | 动态心电分析软件 | 深圳市凯沃尔电子有限公司 | 国械注准20223211142 |
2 | 麻醉机 | 深圳迈瑞生物医疗电子股份有限公司 | 国械注准20223081143 |
3 | 微波治疗机 | 吉林省众驰医疗科技有限公司 | 国械注准20223091144 |
4 | RhD血型检测试剂(渗滤法) | 珠海丽珠试剂股份有限公司 | 国械注准20223401145 |
5 | 恶性疟原虫富组氨酸蛋白Ⅱ(HRP-Ⅱ)抗原检测试剂(胶体金法) | 杭州博拓生物科技股份有限公司 | 国械注准20223401146 |
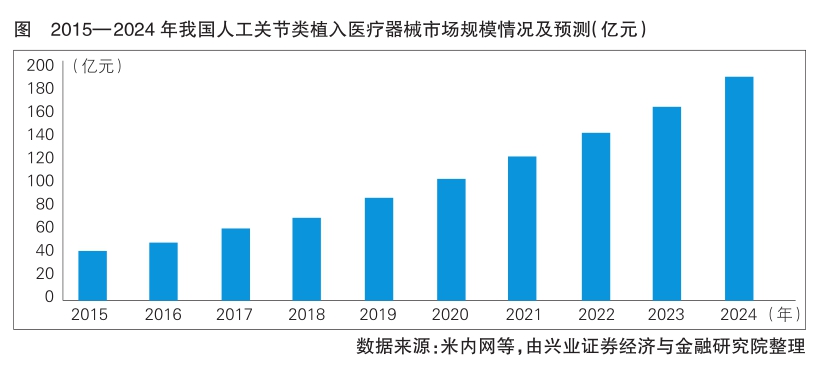
人口老龄化加速我国人工肩关节市场扩张空间大